რა ინგრედიენტები შედის ვაქცინის შემადგენლობაში?
ვაქცინა შეიცავს დაავადების გამომწვევი მიკროორგანიზმის მცირე ზომის ფრაგმენტს ან ამ მცირე ზომის ფრაგმენტის შექმნის პროგრამას. ვაქცინა ასევე შეიცავს სხვა ინგრედიენტებს, რომლებიც აუცილებელია ვაქცინის უსაფრთხოებისა და ეფექტურობისთვის. ამ უკანასკნელ ინგრედიენტებს ვხვდებით ვაქცინების უმრავლესობაში და ათწლეულების მანძილზე ვაქცინების მილიარდობით დოზაში გამოიყენება.
ვაქცინის თითოეული კომპონენტი კონკრეტულ მიზანს ემსახურება და წარმოების პროცესში თითოეული ინგრედიენტი გადის შემოწმებას. ასევე მოწმდება ყველა ინგრედიენტის უსაფრთხოება.
ანტიგენი
ყველა ვაქცინა შეიცავს იმუნური პასუხის გამომწვევ აქტიურ კომპონენტს (ანტიგენტს), ან აქტიური კომპონენტის შესაქმნელ პროგრამას. ანტიგენი შესაძლოა იყოს დაავადების გამომწვევი მიკროორგანიზმის მცირე ზომის ნაწილი, ცილის ან შაქრის მსგავსი, ან მთლიანი მიკროორგანიზმი დასუსტებული ან არააქტიური ფორმით.
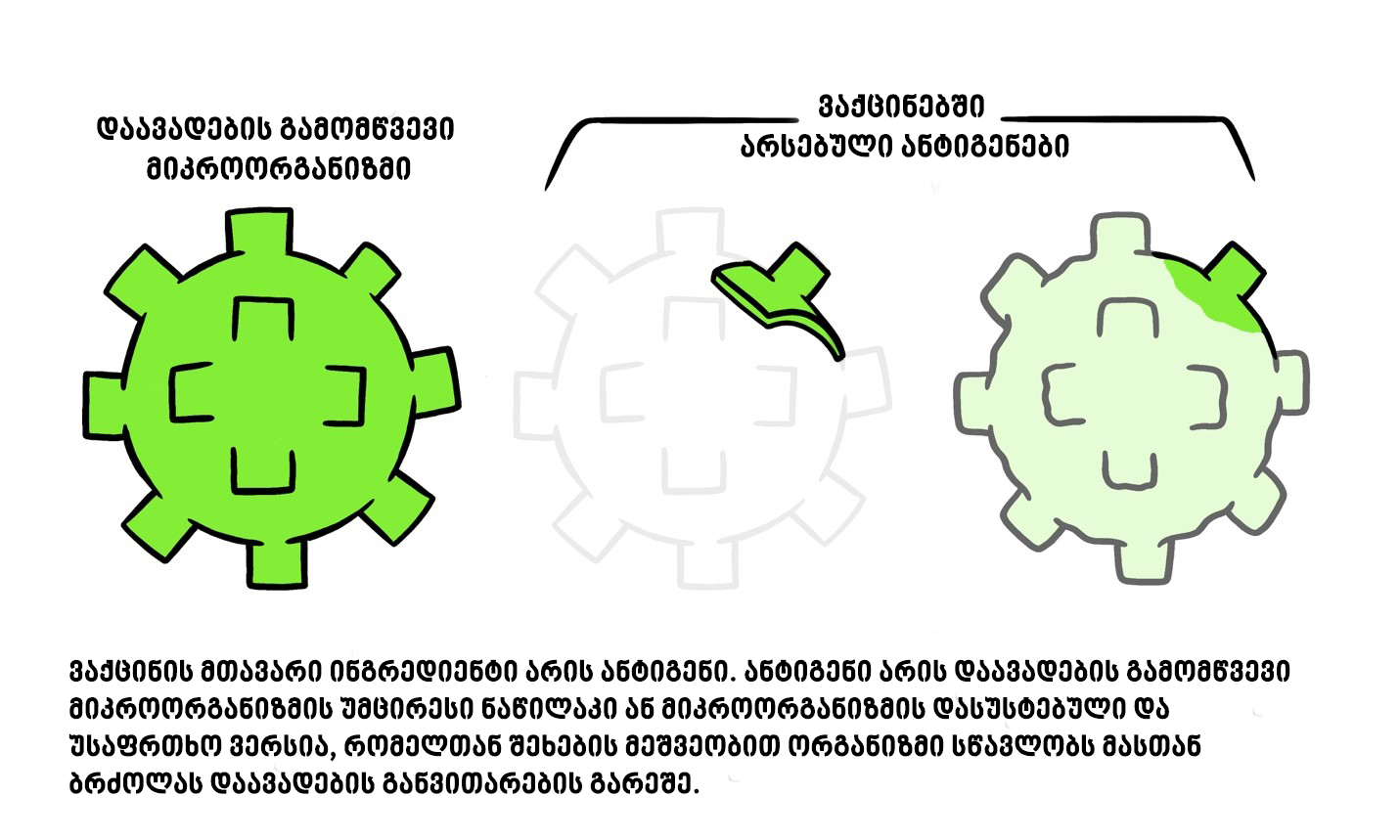
კონსერვანტები
კონსერვანტები უზრუნველყოფენ ფლაკონის გახსნის შემდეგ ვაქცინის კონტამინაციის პრევენციას, თუ ფლაკონში მოთავსებული ვაქცინა ერთზე მეტი ადამიანის აცრისთვის არის გათვალისწინებული. ზოგიერთი ვაქცინა არ შეიცავს კონსერვანტებს, რადგან მათი შენახვა ერთდოზიან ფლაკონებში ხდება და ერთი დოზის გამოყენების შემდეგ ფლაკონი უტილიზაციას ექვემდებარება. ყველაზე ფართოდ გამოყენებადი კონსერვანტს 2-ფენოქსიეთანოლი წარმოადგენს, რომელიც მრავალი წლის განმავლობაში გამოიყენება რიგ ვაქცინებსა და ბავშვის მოვლის საშუალებებში. აღნიშნული კონსერვანტი უსაფრთხოა ვაქცინებში გამოსაყენებლად, რადგან ნაკლებად ტოქსიკურია ადამიანებისთვის.
სტაბილიზატორები
სტაბილიზატორები უზრუნველყოფენ ქიმიური რეაქციების პრევენციას ვაქცინის შიგნით და ვაქცინის კომპონენტებს არ აძლევენ ფლაკონის კედელზე მიკვრის საშუალებას.
სტაბილიზატორი შეიძლება იყოს შაქრები (ლაქტოზა, საქაროზა), ამინომჟავები (გლიცინი), ჟელატინი და ცილები (საფუარის ბაზაზე დამზადებული რეკომბინანტი, ადამიანის ალბუმინი).

სურფაქტანტები (ზედაპირულად აქტიური ნივთიერებები)
სურფაქტანტები უზრუნველყოფენ ვაქცინის ინგრედიენტების შერეულ მდგომარეობაში შენარჩუნებას და ვაქცინაში ლიკვიდურ მდგომარეობაში შემავალი ელემენტების დალექვის და შეწებების პრევენციას. სურფაქტანტები ასევე ხშირად გამოიყენება საკვებ პროდუქტებში, მაგალითად, ნაყინში.
მინარევები
მინარევები სხვადასხვა ნივთიერებების უკიდურესად მცირე ზომის რაოდენობაა, რომლებიც ვაქცინის დამზადების ან წარმოების დროს გამოიყენება და არ წარმოადგენენ დასრულებული ვაქცინის აქტიურ ინგრედიენტებს. ნივთიერებების შეცვლა დამოკიდებულია დამზადების პროცესზე და შესაძლოა შეიცავდეს კვერცხის ცილას, საფუარს ან ანტიბიოტიკებს. აღნიშნული ნივთიერებებისგან დატოვებული კვალი, რომელიც შესაძლოა ვაქცინაში შენარჩუნდეს, იმდენად მცირე რაოდენობისაა, რომ საჭიროა მემილიონედ და მემილიარდედ რაოდენობაში გაზომვა.
გამხსნელი
გამხსნელი არის სითხე, რომელიც ვაქცინის უშუალო გამოყენებამდე შესაბამის კონცენტრაციამდე გაზავებისთვის გამოიყენება. ყველაზე ფართოდ გამოყენებულ გამხსნელს გამოხდილი წყალი წარმოადგენს.
ადიუვანტი
ზოგიერთი ვაქცინა შესაძლოა ასევე შეიცავდეს ადიუვანტებსაც. ადიუვანტი აუმჯობესებს ვაქცინაზე იმუნურ რეაქციას ინექციის წერტილზე ვაქცინის უფრო ხანგრძლივი პერიოდით შენარჩუნების ან ადგილობრივი იმუნური უჯრედების სტიმულირების მეშვეობით.
ადიუვანტი შესაძლოა იყოს ალუმინის მარილების (მაგ.: ალუმინის ფოსფატის, ალუმინის ჰიდროქსიდის ან ალუმინ-კალიუმის სულფატის) მცირე რაოდენობა. დამტკიცებულია, რომ ალუმინი არ იწვევს ხანგრძლივ ჯანმრთელობის პრობლემებს და ადამიანები რეგულარულად იღებენ ალუმინს საკვების და სასმელის მოხმარების პროცესში.
როგორ ხდება ვაქცინების შემუშავება?
ვაქცინების უმეტესობა უკვე ათწლეულების მანძილზე გამოიყენება და ყოველწლიურად მილიონობით ადამიანი უსაფრთხოდ იცრება. ყველა სხვა მედიკამენტის მსგავსად, თითოეულმა ვაქცინამ უნდა გაიაროს ფართომასშტაბიანი და დეტალური შემოწმება, რომლის საფუძველზეც უნდა დადგინდეს ვაქცინის უსაფრთხოება შესაბამისი ქვეყნის ვაქცინაციის პროგრამაში ჩართვამდე.
შემუშავების პროცესში მყოფმა თითოეულმა ვაქცინამ თავდაპირველად უნდა გაიაროს შემოწმების და შეფასების ფაზა, რომლის საფუძველზეც განისაზღვრება თუ რომელი ანტიგენი უნდა იქნას გამოყენებული იმუნური რეაქციის გამოსაწვევად. აღნიშნული წინაკლინიკური გამოცდის ფაზა ადამიანების მონაწილეობის გარეშე მიმდინარეობს. ექსპერიმენტული ვაქცინის გამოცდა თავდაპირველად ხდება ცხოველებზე უსაფრთხოების და დაავადების პრევენციის შესაძლებლობის შემოწმების მიზნით.
თუ ვაქცინა აღძრავს იმუნურ რეაქციას, ამის შემდეგ ხდება მისი შემოწმება ადამიანებზე, კლინიკური გამოცდების ფარგლებში, რომლებიც სამი ფაზისგან შედგება.
პირველი ფაზა
მცირე ჯგუფში შემავალ მოხალისეებს უტარდებათ აცრა ვაქცინიის უსაფრთხოების შეფასების, იმუნური პასუხის წარმოქმნის დადასტურების და სწორი დოზის განსაზღვრის მიზნით. როგორც წესი, აღნიშნული ფაზაში ვაქცინების გამოცდა ხდება ახალგაზრდა და ჯანმრთელ, სრულწლოვან მოხალისეებზე.
მეორე ფაზა
ვაქცინის უსაფრთხოების და იმუნური რეაქციის აღძვრის უნარის შემდგომი შეფასების მიზნით, აცრა უტარდება რამდენიმე ასეულ მოხალისეს. აღნიშნული ფაზის მონაწილეებს გააჩნიათ ისეთივე მახასიათებლები (ასაკი, სქესი), როგორიც ვაქცინის სამიზნე ჯგუფში შემავალ ადამიანებს. ამ ეტაპზე ტარდება რამდენიმე გამოცდა სხვადასხვა ასაკობრივი ჯგუფის და ვაქცინის განსხვავებული შემადგენლობების შესაფასებლად. ამავე ეტაპზე, როგორც წესი, შესადარებელი ჯგუფის სახით გამოცდაში ერთვება ჯგუფი, რომელსაც არ მიუღია ვაქცინა. აღნიშნულ საფუძველზე დგინდება აცრილთა ჯგუფის წევრებში დაფიქსირებული ცვლილებები ვაქცინითაა გამოწვეული თუ შემთხვევითობის შედეგს წარმოადგენს.
მესამე ფაზა
შემდეგ ეტაპზე ხდება ათასობით მოხალისის ვაქცინაცია და შედარება ანალოგიურ ჯგუფში შემავალ მოხალისეებთან, რომელთაც არ მიუღიათ ვაქცინა, თუმცა მიიღეს შესადარებელი პროდუქტი. აღნიშნულის საფუძველზე განისაზღვრება ვაქცინის ეფექტურობა შესაბამისი დაავადებისგან თავდაცვის მიზნით და ხდება ვაქცინის უსაფრთხოების შესწავლა ადამიანთა გაცილებით ფართო ჯგუფზე. უმეტეს შემთხვევაში, გამოცდების მესამე ფაზა ტარდება სხვადასხვა ქვეყანაში და ქვეყნის შიგნით სხვადასხვა ადგილებში, იმის დასადასტურებლად, რომ ვაქცინის ეფექტურობასთან დაკავშირებული მიგნებების გამოყენება შესაძლებელია მოსახლეობის სხვადასხვა ჯგუფთან.
გამოცდების მეორე და მესამე ფაზის დროს, მოხალისეებმა და კვლევაში ჩართულმა მეცნიერებმა არ იციან, რომელმა მოხალისეებმა მიიღეს შესამოწმებლად გამოტანილი ვაქცინა და რომლებმა მიიღეს შესადარებელი პროდუქტი. აღნიშნულს ეწოდება „ბრმა მიდგომა“ და აუცილებელია იმისთვის, რომ მოხალისეები და მეცნიერები ვაქცინის უსაფრთხოების ან ეფექტურობის შეფასებისას, გადაწყვეტილების მიღებისას, არ იმყოფებოდნენ იმ ინფორმაციის ზეგავლენის ქვეშ, თუ ვინ რომელი პროდუქტი მიიღო. გამოცდების დასრულების და ყველა შედეგის მიღების შემდეგ ხორციელდება მოხალისეების და კვლევაში ჩართული მეცნიერების ინფორმირება იმასთან დაკავშირებით, თუ ვინ მიიღო ვაქცინა და ვინ შესადარებელი პროდუქტი.

ყველა ამ კლინიკური გამოცდების შედეგების მიღების შემდეგ, მარეგულირებელი და საზოგადოებრივი ჯანდაცვის პოლიტიკის ნებართვის მოსაპოვებლად საჭიროა მთელი რიგი ნაბიჯების გადადგმა, მათ შორის, ეფექტურობის და უსაფრთხოების მიმოხილვა. თითოეული ქვეყნის უფლებამოსილი პირები ყურადღებით შეისწავლიან კვლევის მონაცემებს და იღებენ გადაწყვეტილებას ვაქცინების გამოსაყენებლად ავტორიზების შესახებ. დამტკიცებამდე და ეროვნული იმუნიზაციის პროგრამაში ჩართვამდე, საჭიროა ვაქცინა აღიარებულ იქნას უსაფრთხო და ეფექტურ საშუალებად მოსახლეობის ფართო ფენებში. ვაქცინის უსაფრთხოების და ეფექტურობის დონე უკიდურესად მაღალია, რადგან ხდება ისეთი ადამიანების აცრა, რომლებიც ჯანმრთელები არიან და არ ავადმყოფებენ იმ დაავადებით, რომლის წინააღმდეგაც მოხდა ვაქცინის შემუშავება.
ვაქცინის დანერგვის შემდეგაც მუდმივი მონიტორინგი მიმდინარეობს. არსებობს სისტემები ნებისმიერი ტიპის ვაქცინის უსაფრთხოების და ეფექტურობის მონიტორინგის მიზნით. აღნიშნული, საშუალებას აძლევს მკვლევარებს თვალი ადევნონ ვაქცინის ზემოქმედებას და უსაფრთხოებას, ადამიანების ფართო ჯგუფებზე გამოყენების დროს და ხანგრძლივი პერიოდის განმავლობაში. მოპოვებული მონაცემები გამოიყენება ვაქცინაციის პოლიტიკის კორექტირების, ასევე ვაქცინის ზემოქმედების ოპტიმიზაციის და გამოყენების პერიოდში ვაქცინის ზემოქმედებაზე უსაფრთხო რეჟიმში დაკვირვების მიზნით.
ვაქცინის გამოყენებაში ჩაშვებისთანავე საჭიროა მუდმივი მონიტორინგის წარმოება, ვაქცინის უსაფრთხოებაში დასარწმუნებლად.
აღნიშნული პუბლიკაცია წარმოადგენს მსოფლიო ჯანდაცვის ორგანიზაციის ვაქცინების შექმნისა და განაწილების შესახებ გამოქვეყნებული განმარტებითი სტატიების მეორე ნაწილს, რომელშიც ყურადღება ეთმობა ვაქცინების შემადგენელ ინგრედიენტებს და კლინიკური გამოცდების სამ ფაზას. პირველ სტატიაში ახსნილია თუ როგორ იცავს ვაქცინა ჩვენს ორგანიზმს დაავადების გადამტანი მიკრობებისგან. მესამე ნაწილი მოიცავს ვაქცინაზე მუშაობის შემდეგ ეტაპს: კლინიკური გამოცდის ფაზის დასრულებიდან განაწილების ჩათვლით.
ორიგინალი სტატია ხელმისაწვდომია აქ.